文章来源:钛媒体
文 | 医曜
前有 「预告式」BD,现有 「诱饵式」 回购,部分创新药公司为了吸引投资者也是拼了。
自 6 月 27 日披露回购方案后,迈威生物至今回购股票数字依然为 0。虽然迈威生物没有任何实质性回购动作,可预期却是卖出去了,公司股价由公告披露当时的 24.11 元,一路飙升至最高 63.59 元。甚至伴随股价的上涨,迈威生物还将当初回购的上限由 35 元提升至 48 元。
一边抬高回购价格上限,一边延迟实际回购动作,而且发生在迈威生物筹划港股 IPO 的关键时期,这种做法值得投资者深思。
01 项庄舞剑,意在沛公
这个回购计划从一开始就充满了戏剧性。
2025 年 6 月,迈威生物承诺以不超过 35 元/股的价格回购 2500 万至 5000 万元股份。然而,在短短一个多月后的 8 月 5 日,迈威生物突然宣布将回购价格上限提升至 48 元/股,比当时 35 元的股价高出 37.14%。
提高回购价格上限通常被视为一家公司对未来信心十足的体现,因此在迈威生物提高回购价格公告之后,刺激了其股价涨幅超 60%,似乎投资者也认可了迈威管理层的做法。
然而,事实情况却是,迈威生物此次股权回购的上限仅为 5000 万元,而最近一段时间迈威生物的每日成交金额均在 20 亿级别,即使迈威生物全部回购,对于迈威生物来说也只是杯水车薪,很难对股价产生太大的影响。因此,迈威生物这种 「只说不做」 的行为模式,更像是为投资者提供的一种 「预期指引」。
「预期指引」 的方向已然十分明确:8 月 31 日,迈威生物公告重新向港交所递交 H 股上市申请。当前,迈威生物市值约 200 亿元,已来到了历史最高峰,若港股发行价按 20% 折让,募资额可达 30 亿元,足以覆盖短期债务,这才是 「小心思」 的核心意图。
目前迈威生物正面临极为严峻的现金流压力。根据 2025 年半年报数据,迈威生物上半年研发费用支出 3.92 亿元,同比增长 21.72%,货币现金虽结余 13.91 亿元,可却有 10.1 亿元的短期负债,资产负债率更是攀升至 77.4%,负债总额高达 34.65 亿元。
若成功上市,迈威生物资金流动性将显著改善,后续通过股权融资、债务置换等方式缓解偿债压力,能极大程度地解除危机。然而,一件不大不小的事,却可能严重影响迈威生物成功登陆港交所。
2025 年 5 月,迈威生物董事长兼总经理刘大涛因涉嫌短线交易被证监会立案调查。经查明,刘大涛于 2022 年 1 月 18 日迈威生物上市至 2022 年 7 月 18 日期间,使用周某证券账户买入、卖出迈威生物股票合计达 3318 万元。对此,监管部门给予刘大涛警告,并处以 60 万元罚款。
尽管这一点点罚款并不会影响迈威生物经营,但港股上市委员会通常对管理层诚信问题零容忍,此类事件可能延长审核周期甚至导致上市中止。因此,迈威生物能否顺利 IPO 还留有悬念。
除资本市场融资外,迈威生物还试图通过债务工具补充资金。2025 年 3 月,其公告拟向中国银行间市场交易商协会申请注册发行不超过 5 亿元的定向债务融资工具,用于偿还有息负债、项目建设及补充流动资金;同时拟向金融机构申请合计不超过 62 亿元的授信/融资额度,较 2024 年 1 月的 23 亿元授信规模大幅提升 169.57%,反映出其对外部资金的依赖度持续增加。
迈威生物当前的多渠道融资举措,本质上是短期流动性 「高压」 之下的的缓解策略,无法从根本上解决 「营收增长乏力-研发投入高企-持续亏损」 的经营闭环问题。对于创新药企而言,长期发展的核心逻辑仍在于在研管线的商业化落地能力。
02 拳头产品不够硬
股市短期是一个投票器,长期则是一台称重机。
无论迈威生物市值管理策略做的多么天花乱坠,但其核心价值却依然要取决于其研发管线和商业化能力。但较为可惜的是,其已上市产品的商业化能力表现并不突出,急需爆款大单品支撑。
截至目前,迈威生物已上市品种有 4 个,包括 3 个生物类似药和 1 个创新药,2025 年上半年贡献营收 1.01 亿元,同比长 53.50%。主要收入来源于地舒单抗 (骨疾病及肿瘤治疗领域) 的 9954.07 万元。
迈利舒 (地舒单抗骨疾病适应症) 于 2023 年 3 月获批上市,是全球第 2 款获批上市的普罗力生物类似药;迈卫健 (地舒单抗肿瘤适应症) 于 2024 年 3 月获批上市,是中国首款获批上市的安加维生物类似药。
作为生物类似药,地舒单抗在国内已经卷起来了。上市品种除了原研药安加维、普罗力和迈威生物的迈利舒、迈卫健外,还有国产生物类似药博安生物的博优倍、博洛加,齐鲁制药的鲁可欣、鲁达欣,康宁杰瑞的恒盖,以及来自石药集团的国产首款 RANKL 单抗创新药纳鲁索拜单抗。单论商业化能力,迈威生物在齐鲁制药、石药集团这种大佬面前,毫无胜算。
迈威生物还有一款生物类似药君迈康 (阿达木单抗),阿达木单抗作为曾经的药王,在其核心专利于 2016 年到期之后,在国内几乎呈泛滥之势。除了原研厂家艾伯维外,还有百奥泰、海正药业、信达生物、复宏汉霖、正大天晴、君实生物、神州细胞、武汉生物制品研究所 8 家企业的阿达木单抗生物类似药获批。
迈威生物于 2025 年 3 月获得上海市药品监督管理局颁发的 《药品生产许可证》(B 证),并于 2025 年 7 月获得国家药品监督管理局批准,君迈康的 MAH 由君实生物变更为迈威生物。但似乎,在一片红海之中,君迈康帮不上迈威生物什么忙。
迈粒生或许还有一战之力。迈粒生是迈威生物具有自主知识产权的新一代长效 G-CSF(高活性改构细胞因子),通用名为注射用阿格司亭α,于 2025 年 5 月获批上市。
G-CSF 是最常见的预防、治疗放化疗引起的中性粒细胞减少症的药物。自 1970 年代以来,G-CSF 产品不断升级换代,目前临床应用呈现一、二代并存的格局。第三代长效 G-CSF 在结构、工艺方面都进行了创新升级,提高了患者治疗依从性。
根据医药魔方 PharmaBI IPM 数据库,2024 年中国肿瘤药物前二十的品牌中,长效 G-CSF 品牌占有三个席位,是肿瘤治疗领域的核心品种之一。从目前来看,G-CSF 的竞争格局也已不容乐观,国内长效 G-CSF 已有 8 款。不过这其中只有亿帆医药的艾贝格司亭α和迈粒生为第三代长效 G-CSF。
不过,第三代长效 G-CSF 目前还处于市场初期阶段,在已形成的固有市场中,完成产品迭代还需要很长一段时间。在这种形势下,迈威生物果断选择变现,于 2025 年 6 月将迈粒生 License-out 给了齐鲁制药,交易总额 5 亿元。这是一个明智的选择,相较于需要花大力气培养商业化渠道,不如交给齐鲁制药这种巨头来得省事,但代价是想象力空间几乎没有了。
如此看来,短期内能改变迈威生物预期的,只剩创新药的大额 BD 了。
03 等待中煎熬
ADC 曾经在国内创新药行业掀起过狂风暴雨,荣昌生物、科伦博泰、百利天恒等重磅 ADC 出海都是数十亿、近百亿的交易总额。宜联生物、映恩生物、普米斯生物这类后起之秀也均获得了跨国 MNC 的认可。但可惜的是,作为在国内 ADC 赛道中占有一席之地的迈威生物,其旗下的 ADC 在研产品始终未能实现大额 BD。
今年 6 月,迈威生物达成了一项金额较高的 BD,与 CALICO 就 9MW3811 签署独家许可协议。迈威生物获得付一次性不可退还的首付款 2500 万美元以及最高达 5.71 亿美元里程碑付款。
然而 9MW3811 并不是 ADC,而是一款迈威生物自主研发的 IL-11 单抗。IL-11 作为 IL-6 家族成员,具有促炎、促纤维化特性,可激活 ERK-mTORC1、JAK-STAT3 通路,导致纤维化同时与衰老标志物 「细胞衰老」 相关。在抗衰老研究的动物试验层面,IL-11 单抗展现出显著的抗衰潜力。
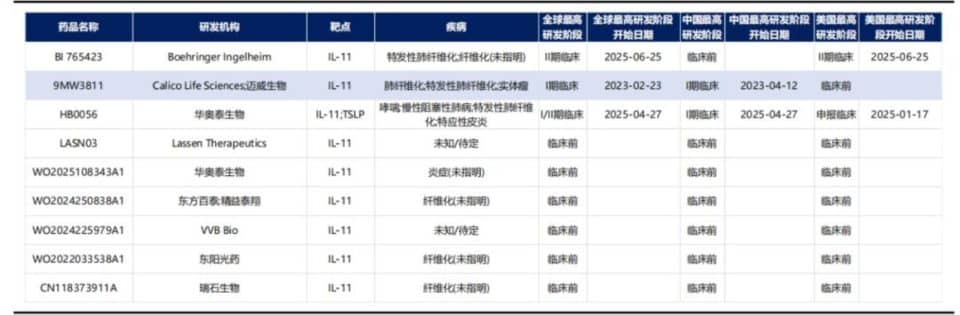
目前全球进入临床的 IL-11 单抗仅三家,其中勃林格殷格翰的 BI 765423 进度最快,于 2025 年 6 月进入治疗肺纤维化的 II 期临床阶段,迈威生物紧随其后,研发进度国内第一,全球前二,目前已获中美澳三个国家的临床准入,其中中国和澳洲临床 I 期已经完成。
图:IL-11 单抗竞争格局,来源:东吴证券
不能说 9MW3811 不够好,但这显然不足以支撑投资者们的强大预期,大家要看到的是迈威生物一系列 ADC 管线的持续 BD 释放。
目前,迈威生物共有 4 款 ADC 产品处于临床阶段,分别是 Nectin-4 ADC(9MW2821)、Trop-2 ADC(9MW2921)、B7-H3 ADC(7MW3711) 和 CDH17 ADC(7MW4911)。其中,7MW4911 已获得美国 FDA 的临床试验许可,尚未获得中国临床试验许可。
9MW2821(Nectin-4 ADC) 是迈威生物的王牌在研产品,已处于临床 III 期,开发进度在尿路上皮癌适应症中位列全球第二,国内第一。并且,9MW2821 已分别于 2024 年 2 月和 5 月先后获得美国 FDA 授予 「快速通道认定」(FTD) 用于治疗晚期、复发或转移性食管鳞癌和 「孤儿药资格认定」(ODD),用于治疗晚期、复发或转移性食管癌;于 2024 年 5 月获得 FDA 授予 FTD 用于治疗既往接受过含铂化疗方案治疗失败的复发或转移性宫颈癌。
7MW3711(B7-H3 ADC) 于 2024 年 7 月获 FDA 授予孤儿药资格认定,用于治疗小细胞肺癌。目前处于Ⅰ/Ⅱ期临床阶段,进度位于国内第二梯队。
9MW2921 是新一代 TROP2 ADC,在 DXd 耐药的多药耐药模型中表现出良好的药效。目前,9MW2921 在中美同时开展了Ⅰ/Ⅱ期临床试验,临床开发进度位于国内第三梯队。
不可否认,迈威生物的这些 ADC 在研竞争力还是不错的,而且其新型抗体偶联技术平台 IDDC 技术能够全面提升 ADC 载药的活性,具有更好的均一性、有效性以及安全性优势。新型载荷 Mtoxin(MF6) 也具有良好的药效、旁观者杀伤效果和抗多药耐药等优势。
单纯从技术能力上看,迈威生物的 ADC 研发能力在国内 Biotech 中名列前茅没有问题。但问题是,这么强劲的实力,何时才能通过 BD 兑现预期呢?尤其是美国极有可能收紧 BD 交易,更增加了迈威生物 ADC 管线 BD 的不确定性。如果单纯的独自融资研发,对于现阶段的迈威生物显然是不符合实际的。
「诱饵式回购」 本质是一场面向港股 IPO 的估值保卫战,通过回购承诺与 BD 叙事维持股价高位,为 H 股发行争取溢价空间。但这些市值管理动作并不会影响公司实质的价值,创新药企的估值还是要看管线厚度与临床数据。
如果一家药企的 PPT 故事比临床数据更精彩时,那才是最骇人的。对于现阶段的迈威生物而言,其核心价值依然还是要看 ADC 管线的 BD 释放预期,而不是所谓的 「回购预期」,衷心期望迈威生物的这份预期可以早日落地。